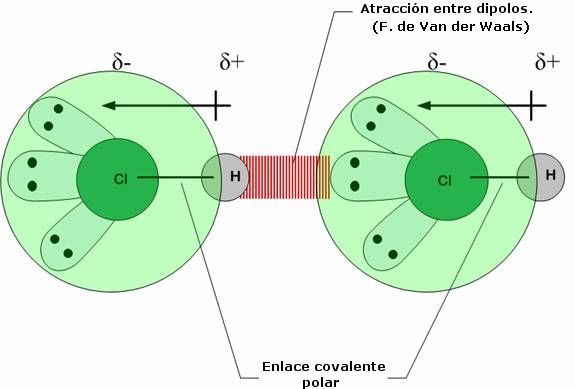
También conocida como Fuerza de Van der Waals, las fuerzas intermoleculares recibieron este nombre en honor al físico que la propuso: Johanes Van der Waals (1837-1923).
Las fuerzas ejercidas entre moléculas (fuerzas intermoleculares) obedecen el estado físico de las sustancias.
Los compuestos moleculares están a temperatura ambiente en los tres estados físicos: sólido, líquido y gaseoso. Este fenómeno se explica por la diferencia en la interacción entre las moléculas, es decir, en cada estado físico ellas se organizan de una forma determinada. Pero en relación al cambio de estado físico, ¿cómo las fuerzas intermoleculares influyen en ese proceso?
La transición de una sustancia de estado sólido a líquido (fusión) o de fase líquida a la fase gaseosa (vaporización), provoca una interrupción de sus moléculas. Las fuerzas intermoleculares se interrumpen durante este proceso debido a la lejanía de las moléculas.
Regla general: cuanto menos intensas sean las fuerzas intermoleculares, más volátil será la sustancia y menor será su temperatura de ebullición (T.E.).
Un compuesto se considera volátil debido a sus interacciones intermoleculares débiles, es decir, las moléculas pueden alejarse llevándolo al estado gaseoso.